- · 《临床药物治疗杂志》编[10/30]
- · 《临床药物治疗杂志》杂[10/30]
- · 《临床药物治疗杂志》杂[10/30]
- · 《临床药物治疗杂志》期[10/30]
- · 《临床药物治疗杂志》数[10/30]
- · 《临床药物治疗杂志》投[10/30]
- · 临床药物治疗杂志版面费[10/30]
重磅发布!《罕见疾病药物临床研发技术指导原(2)
作者:网站采编关键词:
摘要:「由于罕见疾病患者本身临床表现及生理状态等方面差异较大,而关键研究中纳入更加广泛的患者,可能会使研究人群的变异度进一步增加,因此选择敏感
「由于罕见疾病患者本身临床表现及生理状态等方面差异较大,而关键研究中纳入更加广泛的患者,可能会使研究人群的变异度进一步增加,因此选择敏感的主要终点指标、采用更灵活的试验设计,会有助于减少样本量。 」
此外,罕见疾病患者群体年龄跨度较大,可覆盖新生儿至老年患者。针对儿童用药临床研究所面临的伦理、实验效果等挑战,《指导原则》也做了明确规划:
一方面和《儿科人群药物临床试验技术指导原则(2016)》接轨,强调「如果需要在儿童患者中开展研究的,原则上也应首先选择 成人患者,在获得耐受性/安全性,药代动力学,药效动力学(如果可能)后,按照儿童药研发的一般原则,再逐步过渡到青少年和低龄儿童。 」
另一方面「对于极少数无法选择健康成年受试者,疾病人群仅为儿童,无成人患者可选择的特殊情况,也应在充分评估安全性风险的前提下,审慎地考虑在儿童患者开展首次人体试验。 」
产业机会,高效研发路径如何确定
罕见病药物研发的一大商机是罕见疾病药物和常见疾病药物有可能互用。
比如针对罕见病「家族性高胆固醇血症」研究的靶点PCSK9抑制剂,如今被视为21世纪降脂神器。其瞄准的动脉粥样硬化性心血管疾病(ASCVD)是世界上发病率和死亡率最高的疾病之一。
此次《指导原则》中,特别在「临床研发计划」中,针对不同罕见病药物的作用情况做以针对性分析:
「对于适用于包括罕见疾病和非罕见疾病在内的多种疾病的药物,早期可以采用篮式试验设计,纳入多种疾病人群,并充分借鉴、利用在非罕见疾病中获得的临床数据,指导确定该药物在罕见疾病中的开发,根据在其他疾病所获得临床数据对罕见疾病适应症开发的指导价值,可考虑直接开展在罕见疾病适应症中的概念验证临床试验,或直接进入关键临床试验;当直接进入关键临床试验时,可参考前述适应性设计思路。 」
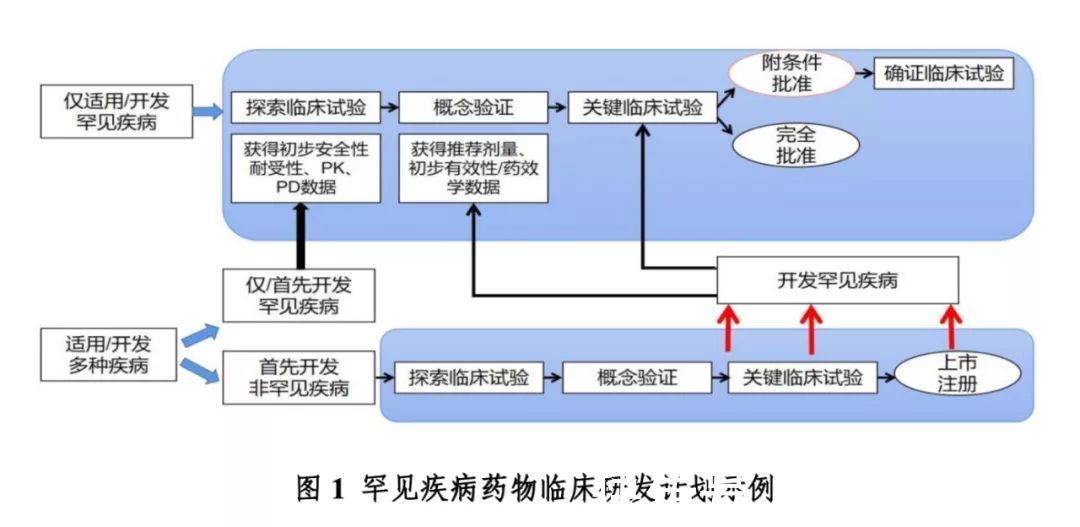
来源:《罕见疾病药物临床研发技术指导原则》
2018年, 由国家卫生健康委员会等五部门联合发布的《第一批罕见病目录》,从官方意义上第一次肯定了中国121种罕见病,开启了此后的中国罕见病药研辉煌——截至目前,中国共60余种罕见病药品,其中已有53种罕见病药品纳入基本医保目录。
可以预见的是,《罕见疾病药物临床研发技术指导原则》发布后,中国罕见病药物研发将进一步规范化。有药企相关负责人对健康界表示出了期待:「其中提到的患者数据的使用、真实世界证据等,都是很好的方向。这个指导原则非常全面了,就坐等未来更多的细则出台。」
2021年11月18日,国家药监局药审中心还对《罕见疾病药物临床研究统计学指导原则(征求意见稿)》公开征求意见。更细分的指导原则开始征求意见,表明「更多细则的拟定已经提上日程」。
政策让中国罕见病药物研发提速,价值有目共睹,下一步改革又将如何深化?请关注健康界后续报道。
来源|健康界
撰文|和星星
文章来源:《临床药物治疗杂志》 网址: http://www.lcywzlzz.cn/zonghexinwen/2022/0110/1673.html